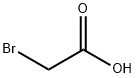
| Sifat Kimia |
JISIM KRISTAL KUNING PUTIH KE PUTIH CAHAYA |
| Kegunaan |
Sintesis organik, abscissi buah sitrus dalam penuaian. |
| Kegunaan |
Asid bromoacetic digunakan dalam sintesis organik dan sebagai agen pengalkilasi. Ia juga digunakan sebagai biokimia untuk penyelidikan proteomik. Ia adalah bahan mentah dan perantaraan penting yang digunakan dalam sintesis organik, farmaseutikal, pewarna dan agrokimia. |
| Kegunaan |
Asid bromoacetic digunakan terutamanya untukN-terminal bromoasilasi peptida terikat resin.
Ia juga boleh digunakan:Untuk mensintesis (Z)-2-(cyclooct-4-en-1-yloxy)asid asetik.
Untuk mensintesis -bromo-phenylacetamide.
Untuk menukar thiosemicarbazones aromatik kepada thiazolylhydrazones.
|
| Penerangan Umum |
Larutan berair. |
| Tindak Balas Udara & Air |
Larut air. |
| Profil Kereaktifan |
Asid karboksilik, seperti ASID BROMOACETIC, menderma ion hidrogen jika terdapat bes untuk menerimanya. Mereka bertindak balas dengan cara ini dengan semua bes, kedua-dua organik (contohnya, amina) dan bukan organik. Tindak balas mereka dengan bes, dipanggil "peneutralan", disertai dengan evolusi sejumlah besar haba. Peneutralan antara asid dan bes menghasilkan air ditambah garam. Asid karboksilik dengan enam atau kurang atom karbon bebas atau sederhana larut dalam air; yang mempunyai lebih daripada enam karbon sedikit larut dalam air. Asid karboksilik larut terurai ke satu tahap dalam air untuk menghasilkan ion hidrogen. Oleh itu pH larutan asid karboksilik adalah kurang daripada 7.0. Banyak asid karboksilik tidak larut bertindak balas dengan cepat dengan larutan akueus yang mengandungi bes kimia dan larut apabila peneutralan menghasilkan garam larut. Asid karboksilik dalam larutan akueus dan cecair atau asid karboksilik cair boleh bertindak balas dengan logam aktif untuk membentuk hidrogen gas dan garam logam. Tindak balas sedemikian berlaku pada dasarnya untuk asid karboksilik pepejal juga, tetapi lambat jika asid pepejal kekal kering. Malah asid karboksilik "tidak larut" mungkin menyerap air yang mencukupi dari udara dan larut secukupnya dalam asid Bromoacetic untuk menghakis atau melarutkan bahagian dan bekas besi, keluli dan aluminium. Asid karboksilik, seperti asid lain, bertindak balas dengan garam sianida untuk menghasilkan gas hidrogen sianida. Tindak balas adalah lebih perlahan untuk asid karboksilik pepejal yang kering. Asid karboksilik tidak larut bertindak balas dengan larutan sianida untuk menyebabkan pembebasan hidrogen sianida gas. Gas dan haba yang mudah terbakar dan/atau toksik dihasilkan oleh tindak balas asid karboksilik dengan sebatian diazo, dithiocarbamates, isosianat, merkaptan, nitrida dan sulfida. Asid karboksilik, terutamanya dalam larutan akueus, juga bertindak balas dengan sulfit, nitrit, tiosulfat (untuk memberikan H2S dan SO3), ditionit (SO2), untuk menghasilkan gas dan haba yang mudah terbakar dan/atau toksik. Tindak balas mereka dengan karbonat dan bikarbonat menghasilkan gas tidak berbahaya (karbon dioksida) tetapi masih panas. Seperti sebatian organik lain, asid karboksilik boleh dioksidakan oleh agen pengoksidaan kuat dan dikurangkan oleh agen penurunan kuat. Tindak balas ini menghasilkan haba. Pelbagai jenis produk boleh didapati. Seperti asid lain, asid karboksilik boleh memulakan tindak balas pempolimeran; seperti asid lain, ia sering memangkinkan (meningkatkan kadar) tindak balas kimia. |
| Bahaya |
Merengsa kuat pada kulit dan tisu. |
| Bahaya Kesihatan |
TOKSIK; penyedutan, pengambilan atau sentuhan (kulit, mata) dengan wap, habuk atau bahan boleh menyebabkan kecederaan teruk, melecur atau kematian. Sentuhan dengan bahan cair boleh menyebabkan melecur teruk pada kulit dan mata. Tindak balas dengan air atau udara lembap akan membebaskan gas toksik, menghakis atau mudah terbakar. Tindak balas dengan air boleh menghasilkan banyak haba yang akan meningkatkan kepekatan wasap di udara. Kebakaran akan menghasilkan gas yang merengsa, menghakis dan/atau toksik. Larian daripada kawalan kebakaran atau air pencairan mungkin menghakis dan/atau toksik dan menyebabkan pencemaran. |
| Bahaya Kebakaran |
Bahan mudah terbakar: boleh terbakar tetapi tidak mudah terbakar. Bahan akan bertindak balas dengan air (sesetengahnya secara ganas) membebaskan gas dan larian yang mudah terbakar, toksik atau menghakis. Apabila dipanaskan, wap boleh membentuk campuran mudah letupan dengan udara: bahaya letupan dalam, luar dan pembetung. Kebanyakan wap lebih berat daripada udara. Mereka akan merebak di sepanjang tanah dan berkumpul di kawasan rendah atau terkurung (pembetung, ruang bawah tanah, tangki). Wap boleh pergi ke sumber pencucuhan dan kilat balik. Sentuhan dengan logam boleh menyebabkan gas hidrogen mudah terbakar. Bekas mungkin meletup apabila dipanaskan atau jika tercemar dengan air. |
| Kemudahbakaran dan Mudah Meletup |
Tidak mudah terbakar |
| Profil Keselamatan |
Racun melalui pengingesan, laluan intraperitoneal dan intravena. Merengsa dan menghakis kulit dan membran mukus. Data mutasi dilaporkan. Apabila dipanaskan hingga mereput ia mengeluarkan asap toksik Br-. Lihat juga BROMIDES. |
| Kaedah Pemurnian |
Menghablurkan asid bromoasettik daripada eter haiwan peliharaan (b 40-60o). Larutan dietil eter daripadanya disalurkan melalui lajur alumina, dan eter disejat pada suhu bilik di bawah vakum. Ia terbaik diperoleh melalui penyulingan daripada Claisen (kelalang yang direndam dalam mandi minyak) yang dipasang dengan lajur Vigreux bertebat (p 11) dan pecahan b 108-110o/30mm dikumpul. Ia sensitif terhadap cahaya dan kelembapan. [Natelson & Gottfried Org Synth Coll Vol III 381 1955, Beilstein 2 IV 526.] LACHRYMATORY dan merengsa kulit. |